瑞途原创 | 从瑞德西韦Ⅲ期临床失败来探讨医药专利实验数据的记载问题
发布日期:2020-04-26
作者:吴雪健、王玉姣、陈彬 | 江苏瑞途律师事务所
(本文约3000字,阅读约需5分钟。)
讨论背景:瑞德西韦Ⅲ期临床失败跌落神坛
自新英格兰医学杂志(NEJM)报道美国第一例新型冠状病毒(2019-nCoV)患者采用瑞德西韦(Remdesivir)进行治疗病情好转[1];同时,中国科学院武汉病毒研究所也发文声称瑞德西韦对抑制2019新型冠状病毒的作用[2],瑞德西韦在新冠肆虐的时期一度成为人们讨论的热点话题,而后瑞德西韦加速进入了临床实验。
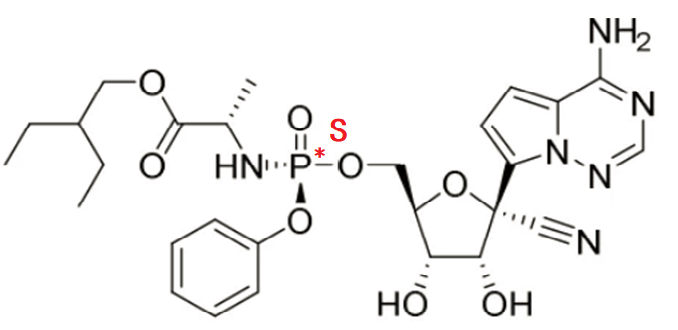
图1 瑞德西韦的绝对构型
然而,就在4月24日世界卫生组织(WHO)挂网发布的摘要显示瑞德西韦Ⅲ期临床试验结果已经出来(随后这篇报道被删除)[3],共有237名患者参与了这项试验,其中159人用药、78人对照。死亡率对比如图2所示,其中用药组的死亡率为13.9%,略高于对照组的12.8%;不良反应率对比如图3所示,其中用药组的不良反应率为65%,略高于对照组的64%;但在药效方面,用药组与安慰剂对照组没有显著性差异,即瑞德西韦对新冠肺炎没有表现出相应的药效,也没能改善患者的病情,瑞德西韦由此跌落神坛。而后,吉利德的股价跌幅一度达到8.5%,创今年3月16日以来最大盘中跌幅[4]。

图2 瑞德西韦用药组/对照组的死亡率对比
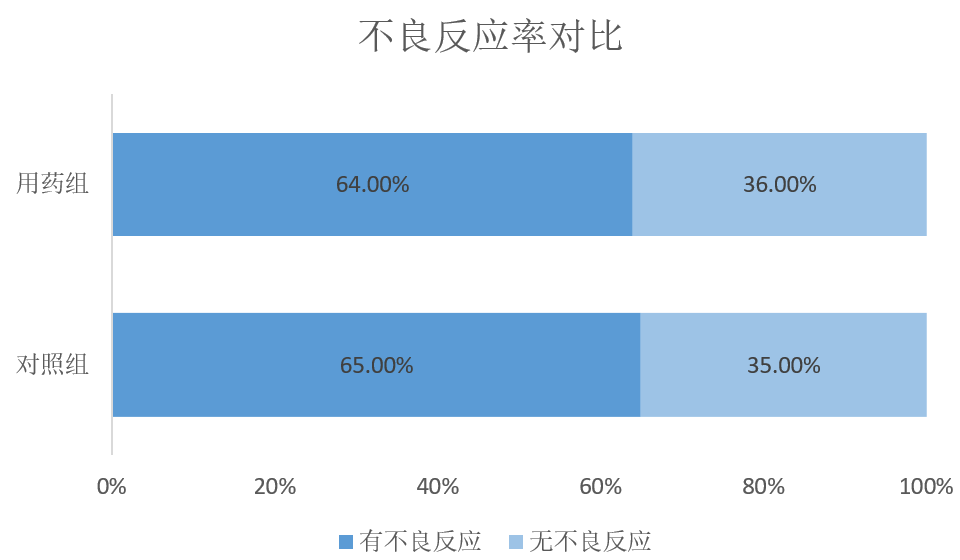
图3 瑞德西韦用药组/对照组的不良反应率对比
为此,药智网的李天泉老师还专门写了《瑞德西韦Ⅲ期临床试验宣告失败,药物有罪推定再显威力》的文章[4];作为一个知识产权的从业人士,笔者脑海中飘过的是医药领域专利保护的问题,由于医药领域的诸多不确定性,特别是治疗用途、药效的不确定性,能否通过补充实验数据来弥补在先申请中的某些缺陷,成为近年来医药领域的争议问题。下面笔者结合自身的实践经验谈一谈实验数据的记载与补充问题。
焦点问题:医药专利的实验数据记载
医药专利在申请的过程中是否应当记载更加充分的实验数据,从而更加充分、严谨地确证新药的有效性;这样是否才能更好地保护具有实际药效价值的创新药?
在我国的医药专利实践中,关于实验数据的记载与补充一直以来都是讨论的热点问题。这是由于医药的研发周期长、成本高和风险大的特点,使得药企之间的竞争非常激烈;为了保证竞争优势,药企通常都会在临床实验前就进行专利申请,此时药企往往尚未对医药的毒性、代谢稳定性和给药途径等进行深入研究;而且,药企之间为了建立技术壁垒、保证竞争优势,即使拥有了相应的实验数据,也往往对部分实验数据进行保留,在进行相应专利申请时并不予以充分公开;更有甚者,大量的医药专利在申请的过程中仅仅记载模糊的技术效果(1993年版的审查指南称之为“含蓄的记载”),并通过后续的行政程序或诉讼程序不断补充实验数据,以维持专利的有效性。
相对于一般的化合物,药品化合物应该具有“医药用途”,这也是药品化合物相对于一般的化合物获得授权的重要条件。虽然,专利审查不能采用“有罪推定原则”,但是由于医药研发属于实验科学,药品化合物是否具有药效往往难以根据其化学结构进行预测。因此,笔者认为,药品专利在申请的过程中应当记载必要的实验数据,以确证化合物的医药用途;同时通过上述必要的实验数据证明该医药专利的创造性。
深入探讨:我国关于医药专利补充实验数据的态度
针对补充实验数据的问题,美国和欧洲对医药专利补充实验数据的政策相对比较宽松;而我国《专利审查指南》由1993年至2017年经历了“含蓄的记载”-“提供”-“记载”-“得到”四个阶段。现在,2017年版的《审查指南》关于补充实验数据的规定为“对于申请日之后补交的实验数据,审查员应当予以审查。补交实验数据所证明的实验效果应当是所属技术领域的技术人员能够从专利申请公开的内容中得到的”。此外,随着2020年1月《中华人民共和国政府和美利坚合众国政府经济贸易协议》的签订[5],我国也可能提高对补充实验数据的接受度。但是,从目前的审判案例来看,我国对医药专利补充实验数据仍然相对严格。
以来那度胺中国专利(申请号:CN97180299.8)的无效及行政诉讼为例,该专利经历了专利无效、行政诉讼一审和行政诉讼二审,最终维持专利权被全部无效的无效决定[6,7]。
该案中证据6(公开号WO1994020085A1)公开了沙利度胺的结构修饰化合物,公开了通式(R4可以为氨基)以及沙利度胺(thalidomide)和其类似物EM-12具有抑制TNFα的作用。因此,合议组认为本专利权利要求1相对于证据6的化合物EM-12区别特征仅在于,本专利化合物在异二氢吲哚环的4位上具有氨基取代基,而证据6的EM-12上该位置是未取代的。
因此,复审委(现在更名为“复审与无效审理部”)认为证据6公开了通式化合物,并限定了取代基团为多种可能,其中包括4位上的R4为氨基的情况,并且将同时所包括的这些化合物作为一类化合物看待。本领域技术人员有动机在母环结构不变的情况下,对末端的取代基团进行常规的结构变换。并且认为变换后的化合物应当具有大体相当的活性水平[6]。
此外,复审委认为本领域技术人员在证据6已经公开EM-12 的基础上,为获得结构类似、活性相当的替代化合物,有动机根据证据6通式化合物部分公开的内容在4位上引入氨基取代基;同时认为,这是本领域技术人员解决获得替代化合物这一技术问题的常规技术手段。并且,由于该结构修饰非常简单,修饰后的化合物与已知化合物EM-12结构差异细微,因此本领域技术人员可以预见该修饰后的化合物与未取代的EM-12具有类似的TNFα抑制活性。并因此认定本领域技术人员在证据6的基础上获得本专利权利要求1的技术方案是显而易见的,本专利权利要求1不符合专利法第22条3款规定的创造性。
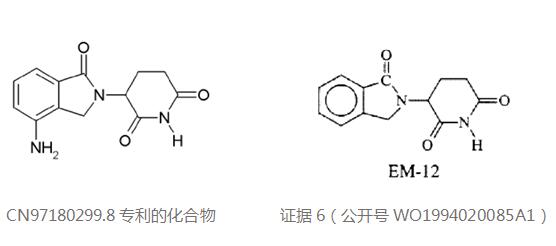
图4 专利化合物与证据6化合物的结构式
为了证明专利的创造性,专利权人在该案中提交了用于证明取得了预料不到的技术效果的实验数据;针对补充提交的实验数据,复审委认为:本案中是否能够补充实验数据,主要看补充后的内容是否为申请文件引入了新的信息。由于我国的发明专利制度采用的是先申请原则,判断专利申请能否授权应以其申请日提交的文件所记载的内容作为基础。并认为如果实验数据是用来证明本专利权利要求1化合物的技术效果实质上优于本领域技术人员所认识到的现有技术的一般水平,例如明显优于证据6中公开的EM-12,则该信息是本领域技术人员在阅读原始申请文件后无法获知的内容,因此复审委未接受专利权人补充提交的实验数据[6]。
结语
由于我国的发明专利制度采用的是先申请原则,针对补充提交的实验数据是否能予以接受,主要需要考虑补充后的内容是否为申请文件引入了新的信息;如果引入的信息是本领域技术人员在阅读原始申请文件后无法获知的内容,则补充提交的实验数据不应当予以接受。
此外,由于医药专利相对于一般的发明创造具有特殊性,其往往直接决定着患者的生与死;而且,由于医药研发属于典型的实验科学,只有通过有效的实验数据才能证明医药相对于一般的化合物具有相应的医疗用途;笔者认为医药专利在申请的过程中应当记载更加充分的实验数据,从而更加充分、严谨的确证新药的有效性。
最后,借用药智网的李天泉老师的那句话,虽然瑞德西韦本次临床试验失败了,我们依然向它致敬!向吉利德科学公司、向瑞德西韦的研究者、向参与试验的志愿者致敬!
[1]Holshue M L, DeBolt C, Lindquist S, et al. First case of 2019 novel coronavirusin the United States. New England Journal of Medicine, 2020.
[2]Wang M, Cao R, Zhang L, et al. Remdesivir and chloroquine effectively inhibitthe recently emerged novel coronavirus (2019-nCoV) in vitro. Cell Research,2020: 1-3.
[3]知识产权律师微信公众号:https://mp.weixin.qq.com/s/MqXx_J1ia_v29tIZ43BtXA
[4] 李天泉.瑞德西韦Ⅲ期临床试验宣告失败,药物有罪推定再显威力,药智网 微信公众号. https://mp.weixin.qq.com/s?__biz=MzAxODA5MTU3NQ==&mid=2650237712&idx=1&sn=69205d0c384ce0fa9056e162bdefc4b0&chksm=83d85048b4afd95e3600e2521a265e62a020e83695e195deb233027b909f8269ed82b1e66656&mpshare=1&scene=1&srcid=&sharer_sharetime=1587699241260&sharer_shareid=188c5666ae5f8818fe788bec459eaaf9&key=86794a6e80bbe80218be9eca4c56bb8fbf7b1c08f266e260c887beb7b9f5de4728ea6023d5f68e0e078e86c1a029fe52d225a9e914da48564882679ea526520e1b9da0b4d209635f14fcf1e99f839c34&ascene=1&uin=MjE4Njk3ODA0MQ%3D%3D&devicetype=Windows+10&version=62080079&lang=zh_CN&exportkey=AVZ8%2FICxE2dVFzetZySsw6M%3D&pass_ticket=jglBfcq0wnwWjfD%2FPGtg3lsiX6z3DSQ7GGe4WUHXCyRI92ZGiFvWx%2FavEH2Qw3ix
[5]商务部新闻办公室,关于发布中美第一阶段经贸协议的公告,中华人民共和国商务部网站:http://www.mofcom.gov.cn/article/ae/ai/202001/20200102930845.shtml
[6]国家知识产权局专利复审委员会:CN97180299.8专利无效决定(决定号第4W101921 号)[7]北京市高级人民法院:赛尔金有限公司与国家知识产权局专利复审委员会其他二审行政判决书(2015年高行(知)终字第00309号)



- 上一篇:瑞途原创 | 名气好借,责任
- 下一篇:瑞途原创 | 人工智能领域的



